Kaliumpermanganat oxidiert Haut, Kleidung und viele anderen Stoffe, es muss sauber gearbeitet werden. Schutzbrillen, Schutzhandschuhe und Schutzkittel sind unbedingt notwendig. Aufgrund der möglichen reprotoxischen Wirkung (Kategorie D 2) wird empfohlen, nur mit erfahrenen Praktikumsteilnehmern Versuche durchzuführen. Werdende oder stillende Mütter dürfen mit diesem Stoff nicht arbeiten. Beim Verschlucken können Vergiftungserscheinungen oder Verätzungen der Schleimhäute auftreten. Kaliumpermanganat ist kein Explosivstoff, kann aber zur Herstellung derartiger Stoffe verwendet werden (rechtlicher Hinweis). Es wird empfohlen, an Schulen ein Bestandsbuch für die vorhandenen Vorratsmengen anzulegen.
Gefährdungsbeurteilungen
GBU Experimentieren mit Kaliumpermanganat-Lösungen
GBU Herstellen von Sauerstoff aus Kaliumpermanganat
Kaliumpermanganat
KMnO4
CAS 7722-64-7
Kaliumpermanganat
Potassium permanganate
158,04 g/mol
0,2 mg/m3 E (TRGS 900)
2,703 g/cm3
+357 °C (Zersetzung +550°C)
100g H2O lösen 6,43 g (L)
0,2 mg/m3 E (TRGS 900)
2,703 g/cm3
+357 °C (Zersetzung +550°C)
100g H2O lösen 6,43 g (L)
Dunkelviolett oder grünlich schimmernde Kristalle

Gefahrenklassen + Kategorie
Oxidierende Feststoffe 2
Akute Toxizität oral 4
Ätzwirkung auf die Haut 1C
Schwere Augenschädigung 1
Reproduktionstoxizität (d) 2
Spez. Zielorgantox. wiederh. 2
Gewässergef. akut/chron. 1
Oxidierende Feststoffe 2
Akute Toxizität oral 4
Ätzwirkung auf die Haut 1C
Schwere Augenschädigung 1
Reproduktionstoxizität (d) 2
Spez. Zielorgantox. wiederh. 2
Gewässergef. akut/chron. 1
Kaliumpermanganat bildet violette oder grün metallisch glänzende Kristalle. Diese lösen sich nur mäßig in Wasser, wobei eine intensiv violette Lösung entsteht. Diese färbt aufgrund ihrer oxidierenden Wirkung Haut und Textilien braun. Dabei entstehen braune, nur schwer entfernbare Mangan(IV)-oxid-Flecken. Auf der Haut sind die Flecken nach ein paar Tagen abgebaut, auf Textilien bleiben sie dauerhaft. Kaliumpermanganat zerstört Geruchsstoffe und wirkt bakterientötend.

Kaliumpermanganat-Kristalle glänzen violett oder schimmern grün metallisch.
Die kräftige, violette Farbe in Lösungen wird durch das Permanganat-Anion verursacht, das in der Oxidationsstufe +VII vorliegt. Legt man ein paar Kristalle Kaliumpermanganat an den Grund einer Lösung durchfärbt sich die Lösung nach und nach, ohne dass dabei die Flüssigkeit bewegt wird. Dieses Phänomen der selbständigen Durchmischung verschiedener Stoffe nennt man Diffusion:
Oberhalb von 240 °C erfolgt Zersetzung unter Sauerstoff-Abspaltung. Man erhält Kaliummanganat, Manganit und Sauerstoff. Führt man diese Reaktion in einem Reagenzglas durch, lässt sich der Sauerstoff mit Hilfe der Spanprobe nachweisen.
Mit Salzsäure reagiert Kaliumpermanganat unter Chlorgasentwicklung:
Mit brennbaren oder stark reduzierend wirkenden Stoffen entstehen explosionsgefährliche Mischungen. Mischungen mit fein verteiltem Magnesium oder Aluminium reagieren explosionsartig unter grellem Lichtblitz. Mit Glycerin, Ethylenglykol, Mannit, Acetaldehyd erfolgt Selbstzündung.

Kaliumpermanganat-Kristalle glänzen violett oder schimmern grün metallisch.
Die kräftige, violette Farbe in Lösungen wird durch das Permanganat-Anion verursacht, das in der Oxidationsstufe +VII vorliegt. Legt man ein paar Kristalle Kaliumpermanganat an den Grund einer Lösung durchfärbt sich die Lösung nach und nach, ohne dass dabei die Flüssigkeit bewegt wird. Dieses Phänomen der selbständigen Durchmischung verschiedener Stoffe nennt man Diffusion:
Oberhalb von 240 °C erfolgt Zersetzung unter Sauerstoff-Abspaltung. Man erhält Kaliummanganat, Manganit und Sauerstoff. Führt man diese Reaktion in einem Reagenzglas durch, lässt sich der Sauerstoff mit Hilfe der Spanprobe nachweisen.
10 KMnO4  3 K2MnO4 + 2 K2O • 7 MnO2 + 6 O2
3 K2MnO4 + 2 K2O • 7 MnO2 + 6 O2
Mit Salzsäure reagiert Kaliumpermanganat unter Chlorgasentwicklung:
2 KMnO4 + 16 HCl  5 Cl2 + 8 H2O + 2 MnCl2 + 2 KCl
5 Cl2 + 8 H2O + 2 MnCl2 + 2 KCl
Mit brennbaren oder stark reduzierend wirkenden Stoffen entstehen explosionsgefährliche Mischungen. Mischungen mit fein verteiltem Magnesium oder Aluminium reagieren explosionsartig unter grellem Lichtblitz. Mit Glycerin, Ethylenglykol, Mannit, Acetaldehyd erfolgt Selbstzündung.
Kaliumpermanganat ist in einem mehrstufigen Prozess aus Braunstein und Kaliumhydroxid zugänglich:
Das so erhaltene Kaliummanganat(VI) wird anschließend in wässriger Kalilauge gelöst und elektrochemisch an Nickel-Anoden zu Kaliumpermanganat oxidiert.
Braunstein + Kaliumhydroxid + Sauerstoff  Kaliummanganat(VI) + Wasser
Kaliummanganat(VI) + Wasser
Das so erhaltene Kaliummanganat(VI) wird anschließend in wässriger Kalilauge gelöst und elektrochemisch an Nickel-Anoden zu Kaliumpermanganat oxidiert.
Im Chemieunterricht wird Kaliumpermanganat für Demonstrationsversuche verwendet, beispielsweise:

Osmose: Ein Dialyseschlauch ist für die Wasser-Moleküle und die Kaliumpermanganat-Ionen
durchlässig. Er ist semipermeabel, größere Moleküle wie die von Zucker kommen nicht durch.
Kaliumpermanganat wird bei organischen Reaktionen und Synthesen als Oxidationsmittel häufig benötigt. Bei der Wasseraufbereitung dient es zur Entfernung von Mangan. Bei der Maßanalyse dient es zur Bestimmung von zahlreichen Substanzen. In der Medizin wird es als Desinfektionsmittel und als Gegengift bei Vergiftungen mit Cyanid, Blausäure, Opium, Morphium, Phosphor und bei Schlangenbissen eingesetzt. Es eignet sich auch als Fungizid und Bakterizid für Obstbäume oder Olivenbäume. Früher stellte man aus Kaliumpermanganat und Magnesiumpulver eine explosive Mischung her, die mit einem grellen Lichtblitz abbrannte. Dieses Blitzlichtpulver war der Vorläufer des modernen Elektronenblitzes für die Fotografie.
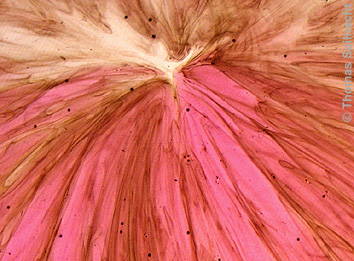
Bei der Reaktion einer mit Schwefelsäure angesäuerten Kaliumpermanganat-Lösung mit 30%iger
Wasserstoffperoxid-Lösung werden die Mn(VII)-Ionen zu (farblosen) Mn(II)-Ionen reduziert.
Medien und Experimente
Experimente zur Geschwindigkeit chemischer Reaktionen
Versuch zum Herstellen von Sauerstoff aus 1g Kaliumpermanganat
Demoversuch (nur als Film empfohlen): Chlor aus Kaliumpermanganat und Salzsäure herstellen
Kaliumpermanganat reagiert mit Glycerin
-
Herstellen von Sauerstoff durch Erhitzen von Kaliumpermanganat
-
Demonstrieren der Diffusion in Flüssigkeiten
-
Demonstrieren der Osmose mit Hilfe eines Dialyseschlauchs
-
Lösungsprozess des farbigen Salzes in Wasser
-
Vergleich der Reaktionsgeschwindigkeit beim Löseprozess in kaltem und warmem Wasser
-
Reaktionsgeschwindigkeit beim Entfärben einer Kaliumpermanganat-Lösung mit Wasserstoffperoxid
-
In der chemischen Analyse zur Bestimmung von Stoffen, beispielsweise von Glucose
- Das Herstellen von Chlor durch die Reaktion mit konzentrierter Salzsäure und die Reaktion von Glycerin mit Kaliumpermanganat wird heute nur noch bedingt für Schulen empfohlen.
Osmose: Ein Dialyseschlauch ist für die Wasser-Moleküle und die Kaliumpermanganat-Ionen
durchlässig. Er ist semipermeabel, größere Moleküle wie die von Zucker kommen nicht durch.
Kaliumpermanganat wird bei organischen Reaktionen und Synthesen als Oxidationsmittel häufig benötigt. Bei der Wasseraufbereitung dient es zur Entfernung von Mangan. Bei der Maßanalyse dient es zur Bestimmung von zahlreichen Substanzen. In der Medizin wird es als Desinfektionsmittel und als Gegengift bei Vergiftungen mit Cyanid, Blausäure, Opium, Morphium, Phosphor und bei Schlangenbissen eingesetzt. Es eignet sich auch als Fungizid und Bakterizid für Obstbäume oder Olivenbäume. Früher stellte man aus Kaliumpermanganat und Magnesiumpulver eine explosive Mischung her, die mit einem grellen Lichtblitz abbrannte. Dieses Blitzlichtpulver war der Vorläufer des modernen Elektronenblitzes für die Fotografie.
Bei der Reaktion einer mit Schwefelsäure angesäuerten Kaliumpermanganat-Lösung mit 30%iger
Wasserstoffperoxid-Lösung werden die Mn(VII)-Ionen zu (farblosen) Mn(II)-Ionen reduziert.
Medien und Experimente
Experimente zur Geschwindigkeit chemischer Reaktionen
Versuch zum Herstellen von Sauerstoff aus 1g Kaliumpermanganat
Demoversuch (nur als Film empfohlen): Chlor aus Kaliumpermanganat und Salzsäure herstellen
Kaliumpermanganat reagiert mit Glycerin
© Thomas Seilnacht / Benutzerhandbuch / Lizenzbestimmungen / Impressum / Datenschutz / Literaturquellen