| Antimon 51Sb | ||||||
| engl. Antimony; arab. Anthos Ammonos („Blüte des Gottes Ammon“) | ||||||
|
Das silbrig glänzende, graue
Antimon ist die
metallische Modifikation des Elements. Im Vergleich zum Arsen ist der Metallcharakter ausgeprägter. Antimonstücke lassen sich
aufgrund der
geringen Härte und ihrer Sprödigkeit leicht
pulverisieren. Das
Metall ist kein besonders guter Leiter für Wärme und
Strom. Wie bei Wasser, Bismut, Gallium und Germanium tritt beim Erstarren von der flüssigen zur festen Zustandsform eine Ausdehnung auf.
Das amorphe, schwarze Antimon erhält man, wenn man Antimondämpfe an kalten
Flächen abschreckt. Diese Modifikation ist sehr reaktionsfähig.
Beim erneuten Erhitzen erhält man wieder das metallische, graue Antimon. Auf
elektrolytischem Weg ist das amorphe, glasartige Antimon zugänglich.
Diese Modifikation ist sehr instabil und explodiert bereits durch Ritzen oder durch schnelles Erhitzen. Unter Aufglühen entsteht auch hier wieder graues Antimon. Graues Antimon ist an der Luft und im Wasser beständig.
Wenn man ein Stück metallisches Antimon im Reagenzglas erhitzt, reagiert das Antimon am Anfang mit dem im Reagenzglas vorhandenen Luftsauerstoff je nach Temperatur zu verschiedenen Antimonoxiden. Der weiße Beschlag besteht aus Antimon(III)-oxid Sb2O3 und aus Antimon(III,V)-oxid Sb2O4, der gelbe Beschlag enthält Antimon(V)-oxid Sb2O5. Beim Erhitzen von metallischem Antimonpulver mit Sauerstoff verbrennt es mit weißlich-blauer Flamme zu Antimon(III)-oxid:
4 Sb + 3 O2 Mit den Halogenen reagiert Antimon zu den entsprechenden Halogeniden. Fein verteiltes Antimonpulver reagiert mit Chlor zum Beispiel unter Aufglühen zu Antimon(V)-chlorid: 2 Sb + 5 Cl2 Mit nicht oxidierenden Säuren wie Salzsäure reagiert Antimon nicht. Mit Salpetersäure erfolgt eine Oxidation zu Antimoniger Säure oder Antimonsäure. Die Marsh-Probe verläuft beim Prüfen auf Antimon positiv, weil sich dabei Antimonwasserstoff bildet, der an der Porzellanschale Antimon abscheidet und einen grauschwarzen Belag erzeugt. Im Gegensatz zum Arsen löst sich der Belag aber in ammoniakalischer Wasserstoffperoxid-Lösung. Antimonwasserstoff ist auch unter dem Namen Monostiban SbH3 bekannt. Er verhält sich chemisch ähnlich wie Arsenwasserstoff und ist ebenfalls stark toxisch. Unedle Metalle wie Eisen oder Zink scheiden in Lösungen mit Antimon(III)- und Antimon(V)-verbindungen schwarze, metallische Antimonflitter oder Antimonflocken ab. Diese Reaktion ist typisch für Antimonverbindungen. |
Antimonstäube
reizen die Schleimhäute und die Augen, elementares Antimon ist
aber nicht besonders toxisch. Das Metall kann vermutlich Krebs erzeugen. Das toxische Potenzial der Verbindungen ist erheblich
höher. Die Antimonchloride verursachen Verätzungen der Haut und
Augenschäden, Antimon(III)-oxid erzeugt vermutlich Krebs, einige Antimonverbindungen
gelten als umweltgefährlich. Antimonwasserstoff ist ein widerwärtig riechendes und extrem toxisches Gas. |
Häufigkeit selten
Antimon ist auf der Erde ein seltenes Element, es ist aber etwa fünfmal so häufig wie Silber. In elementarer Form tritt es als Antimon gediegen auf. Es bildet sich in der Natur durch Reduktion aus dem Mineral Antimonit und ist mit diesem gerne vergesellschaftet.
Viel häufiger treten
jedoch Antimonminerale auf, von denen mehr als 100 bekannt sind. Das wichtigste
Antimonerz ist der nach dem orthorhombischen System kristallisierende Stibnit (Antimonit). Antimon(III)-sulfid bildet neben dem Stibnit noch die rote, amorphe Modifikation Metastibnit. Die Minerale Senarmontit und Valentinit stellen zwei Modifikationen des Antimon(III)-oxids dar. Auch der Tetraedrit und der Pyrargyrit gehören zu den Antimonmineralen.
Die größten abbaufähigen Antimonerzressourcen liegen vor allem
in China, aber auch in Russland, Bolivien oder Kirgisistan kommen Antimonerze reichlich vor. Auch einige andere Länder wie Australien, die Türkei, Kanada oder die USA besitzen abbauwürdige Vorkommen.
|
Antimon
gehört zu den zehn Elementen, die bereits im Altertum bekannt waren.
Schon in der Antike
wurden Antimonpräparate medizinisch verwendet. Pulverisiertes Antimon(III)-sulfid diente aufgrund seiner bakterientötenden Wirkung zur Herstellung von
Augencremes und zur Behandlung von Wunden und Geschwüren. Im alten
Ägypten wurde es auch zur Herstellung von schwarzer Augenschminke
verwendet. Im 16. Jahrhundert führte Paracelsus die innere Anwendung
von den Antimonverbindungen ein. In stark verdünnter Form sollten
sie abführend, schweißtreibend oder als Brechmittel wirken. Diese Anwendung war bei den Ärzten aufgrund der Giftigkeit der Verbindungen jedoch umstritten.
Bei den Alchemisten kam dem Antimon eine besondere Bedeutung zu. Sie nahmen eine Verwandtschaft zum Blei an und verwendeten es zur Scheidung von Gold und Silber. Bei der Zugabe von Antimonsulfid zu einer Gold-Silberlegierung scheidet sich am Boden eine Gold-Antimon-Legierung ab. Beim Erhitzen dieser Legierung verbrennt das Antimon zu Antimon(III)-oxid, so dass reines Gold zurückbleibt. Daher besaß das Antimon in der Alchemie auch Bezeichnungen wie lupus metallorum („Wolf der Metalle“), balneum regis („Königsbad“) oder ludex ultimus („letzter Richter“). Dem Antimon war in der Alchemie das Erdsymbol zugeordnet (erstes Symbol von links): 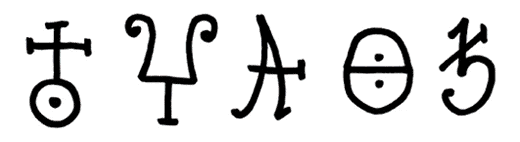 Der Name des lateinischen Wortes stibium für Antimon leitet sich von altägyptischen Wörtern
für schwarze Schminke ab. Der Name Antimon geht auf eine frühere
Bezeichnung des Minerals Antimonit zurück. Das chemische Symbol Sb (lat. stibium) vergab J.J. Berzelius im Jahre 1814. |
Liegen Erze vor, die viel Antimonit enthalten, kann man diese unter Luftabschluss auf etwa 550 °C erhitzen, so dass das niedrig schmelzende Antimon(III)-sulfid in angereicherter Form herausfließt. Meistens hat man aber Erze vorliegen, die nur einen geringen Anteil Antimonerz enthalten. Häufig fällt Antimonsulfid als Nebenprodukt bei der Goldgewinnung an. Zur Metallgewinnung sind drei Verfahren von Bedeutung:
1.) Röstreduktionsverfahren:
Durch das Rösten mit Sauerstoff entsteht
Diantimontetraoxid, das mit Koks oder Holzkohle reduziert wird.
Sb2S3 + 5 O2 Sb2O4 + 4 C 2.) Röstreaktionsverfahren: Das Antimonsulfid wird nur teilweise geröstet und das gebildete Diantimontetraoxid mit übrig bleibendem Antimonsulfid reduziert: Sb2S3 + 5 O2 3 Sb2O4 + 2 Sb2S3 3.) Niederschlagsverfahren:
Durch eine Redoxreaktion mit Eisen erhält man ebenfalls metallisches Antimon:
Sb2S3 + 3 Fe Die Reinigung des Antimons
erfolgt durch die Zugabe von Soda und durch nachfolgendes Schmelzen in
einem Ofen. Sehr reines Antimon erhält man durch elektrolytische Raffination
oder durch die Reduktion von Antimon(III)-chlorid mit Wasserstoff. |
Aufgrund
seiner Sprödigkeit besitzt das Element nur eine geringe technische
Bedeutung. Es lässt sich weder walzen noch ziehen oder prägen.
Antimon dient hauptsächlich als Legierungsbestandteil zur Härtung
anderer weicher Metalle wie Blei, Kupfer, Zinn oder Zink. Früher
bestanden die Drucklettern für den Zeitungsdruck aus einer Antimon-Blei-Legierung.
Heute enthält der Bleischrot für Flinten noch Antimon und Arsen als Legierungsbestandteil. Sehr reines Antimon wird auch in Halbleitern
verwendet. Antimonverbindungen wie Antimonweiß Sb2O3 wurden
früher als Pigmente eingesetzt. Da sie im Verdacht stehen Krebs zu
erzeugen, werden sie heute nicht mehr eingesetzt. In der Medizin
verabreicht man organische
Antimonpräparate zur Chemotherapie bei tropischen
Erkrankungen durch
Einzeller, so auch bei der gefürchteten Schlafkrankheit.
|
|