
|
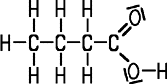
Klare, ölige Flüssigkeit Vorkommen Darm, Fußschweiß, saure Milch |
Molmasse
88,106 g/mol
AGW keine Angaben pKs-Wert +4,83 Dichte 0,9528 g/cm3 Schmelzpunkt −5,12 °C Siedepunkt +163,7 °C Wasserlöslichkeit vollst. mischbar Explosionsgrz. 2,0 bis 10 Vol.-% (Luft) Flammpunkt +72 °C Zündpunkt +443 °C |
| Piktogramme
GHS 05 GHS 07 Gefahr |
Gefahrenklassen
+ Kategorie
Akute Toxizität oral 4 Ätzwirkung auf die Haut 1B Schwere Augenschädigung 1 (Abstufung bei Verdünnungen) |
HP-Sätze
(siehe auch Hinweis)
H 302, 314 P 260, 280.1-3,7, 303+361+353, 304+340+310, 305+351+338+310 Entsorgung G 1 |
| Etikett drucken | Dt. Bezeichnung
Synonyme (deutsch) |
Engl. Bezeichnung
Synonyme (engl.) |
| CAS 107-92-6 | Buttersäure
Butansäure |
Butyric acid
Butanoic acid |
|
Bemerkungen
für Schulen: Buttersäure ist ein ätzender Stoff. Das
Tragen von Schutzbrille und
Schutzhandschuhen ist vorgeschrieben. Es ist auf eine gute
Raumlüftung
zu achten oder im Abzug zu arbeiten. Ein Teflonverschluss verhindert das
Ausdampfen aus der Flasche weitgehend. Das Arbeiten mit
Buttersäure wird
nur für erfahrene Praktikumsteilnehmer empfohlen, da der Stoff
extrem penetrant riecht.
Eigenschaften Buttersäure riecht
äußerst unangenehm und widerlich nach "Erbrochenem". Die Dämpfe
reizen die Augen und die Atemwege. Buttersäure entsteht beim Ranzigwerden
von Butter. Sie löst sich sehr gut in Wasser und auch in Ethylalkohol,
Diethylether und Glycerin.
Die Carbonsäure
ist im Vergleich zur Ameisensäure und Essigsäure
eine schwächere Säure. Eisen,
Zink, Magnesium
und andere unedle Metalle lösen sich unter Wasserstoffentwicklung
ganz langsam auf. Dabei bilden sich die Salze der Buttersäure, die
Butyrate, die bei Feuchtigkeit ebenfalls nach Buttersäure riechen:
Magnesium + Buttersäure Mit Alkoholen
können Ester erzeugt werden. Für
diese Reaktion ist Wärme und ein Katalysator
wie Schwefelsäure notwendig:
Buttersäure + Ethanol Erstaunlicherweise entsteht
ein Ester mit einem gut riechenden Ananasgeruch, der in der Parfümindustrie
und zur Likörherstellung verwendet wird.
|
| Herstellung
Die Herstellung erfolgt
durch die Oxidation von Butanol und Luft unter Zuhilfenahme von geeigneten
Katalysatoren oder durch eine Oxo-Synthese
aus Propen und Kohlenstoffmonooxid.
Von Bedeutung ist auch die Vergärung von Kohlenhydraten durch Clostridium-Bakterien:
C6H12O6 |
| Verwendung
Buttersäure
dient zur Herstellung von Buttersäureestern, Medikamenten,
Schädlingsbekämpfungsmitteln und Cellulosebutyrat, einem
witterungsbeständigen und schlagfesten Kunststoff.
|