|
 Farbloses Gas |
Molmasse 42,080 g/mol AGW keine Angaben Dichte 1,9138 g/l (Gas, 0° C, 1013 hPa) (Propylen zu Luft = 1,48) Schmelzpunkt −185,19 °C Siedepunkt −47,6 °C Wasserlöslk. Konz. bei 25 °C 0,200 g/l Explosionsgrz. 2 bis 11,1 Vol.-% (Luft) Flammpunkt −108 °C Zündpunkt +455 °C |
| Piktogramme GHS 02 GHS 04 Gefahr |
Gefahrenklassen
+ Kategorie Entzündbare Gase 1 Gase unter Druck, verdicht. Gas |
HP-Sätze (siehe Hinweis) H 220, 280 P 210, 280.3, 377, 381, 410+403 Entsorgung besondere Hinweise |
| Dt. Bezeichnung Synonyme (deutsch) |
Engl. Bezeichnung Synonyme (engl.) |
|
| CAS 115-07-1 | Propylen Propen |
Propylene Propene |
| Eigenschaften Das farblose Gas ist
geruchlos, wenig giftig und wirkt aber in höheren Konzentrationen
narkotisierend und erstickend. Es löst sich wenig in Wasser, in Ethylalkohol
und Essigsäure ist es dagegen sehr gut löslich. Propylen brennt
mit gelber, rußender Flamme und bildet mit Luft explosionsfähige
Gemische. Der ungesättigte Kohlenwasserstoff addiert aufgrund seiner Doppelbindung gerne Wasserstoff oder Halogene an sein Molekül:
Propen + Brom Diese Reaktion kann auch
als Nachweisreaktion für das
Vorhandensein von ungesättigten Verbindungen, von Doppel- und Dreifachbindungen
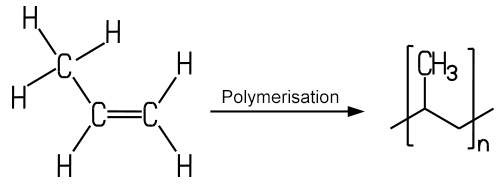
in organischen Stoffen herangezogen werden. Durch eine Polymerisationsreaktion lässt sich der Kunststoff Polypropylen herstellen:
|
| Herstellung Propylen entsteht neben Ethylen und Acetylen in großen Mengen beim thermischen
Cracken von Kohlenwasserstoffen. |
| Verwendung Propylen ist zusammen mit Ethylen eines der wichtigsten Zwischenprodukte der organischen Chemie. Eine bedeutende Verwendung ist die Synthese von Isopropylalkohol, aus dem auch Aceton gewonnen werden kann. Die Addition von Wasser an das Propylen erfolgt mit Hilfe eines Katalysators unter hohem Druck und bei niedrigen Temperaturen: 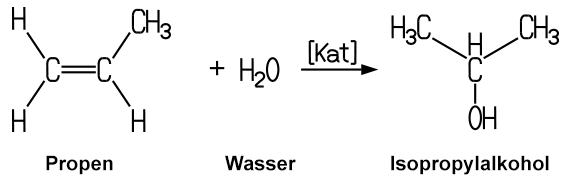 Propylen dient auch zur Herstellung des Kunststoffes Polypropylen und der Kunstfaser Polyacrylnitril, zur Propylenoxid- und Benzolgewinnung, zur Synthese von Acrolein und Allylchlorid, damit auch von Glycerin, sowie zusammen mit Benzol zur Synthetisierung von Cumol. Aus diesem wird wiederum Aceton und Phenol hergestellt. |