| Zinn 50Sn | ||||||
| engl. Tin; lat. stannum („Zinn“) | ||||||
|
|
Zinn
ist ein silbrig glänzendes und relativ weiches Schwermetall.
Es lässt sich mit einem Messer leicht ritzen, und man kann es zu hauchdünnen
Folien auswalzen, die man früher „Stanniol“ nannte. Zinn ist aber nicht ganz so
weich wie Blei. Das knisternde
Geräusch, das beim Verbiegen einer Stange aus Reinzinn entsteht,
wird als „Zinngeschrei“ bezeichnet. Reines
Zinn hat einen relativ niedrigen Schmelzpunkt, weshalb man es
bereits mit einer Kerzenflamme schmelzen kann. Das Zinngießen ist
ein beliebter Brauch an Silvester. Die im Wasser abgekühlten Figuren
gelten als Glücksbringer für das folgende Jahr.
Vom Zinn sind drei Modifikationen bekannt: Bei 13,3 °C geht das graue, kubisch orientierte α-Zinn in weißes tetragonal orientiertes β-Zinn
über. Oberhalb von 162 °C wird das Zinn spröde
und man erhält rhombisch orientiertes, halbmetallisches γ-Zinn,
das beim Herunterfallen in Stücke zerspringt oder im
Mörser zu
einem grauen Pulver zerrieben werden kann.
Die Zinnpest an alten Orgelpfeifen entsteht beim α-Zinn unter Kälte. Diese Modifikation besitzt bei geringen Temperaturen die unangenehme Eigenschaft, dass es allmählich zu einem grauen Pulver zerfällt. Durch das Legieren mit anderen Metallen wie mit Antimon, Bismut oder Blei kann dieses Phänomen weitgehend verhindert werden. Verunreinigungen mit korrosiv wirkenden Metallen wie Mangan oder Zink verstärken dagegen den Vorgang. Bei Zimmertemperatur ist Zinn gegen Luft und Wasser beständig, da es sich allmählich mit einer dünnen Oxidschicht überzieht, die das darunter liegende Metall vor weiterer Korrosion schützt. Beim Erhitzen auf etwa 1500 °C verbrennt Zinnpulver mit dem Luftsauerstoff mit heller Lichterscheinung zu Zinn(IV)-oxid: Sn + O2 Sn + 2 HCl
Mit konzentrierter Salpetersäure
reagiert Zinn unter Bildung von Stickstoffdioxid zu Zinnsäure,
einem glasigen Pulver. Mit Laugen entstehen Hexahydroxostannate. Zinnwasserstoff oder Monostannan SnH4 ist ein toxisches Gas, das bei 150 °C spontan zerfällt. Als typische Nachweisreaktion für Zinn-Ionen kann beispielhaft die Reaktion einer Goldchlorid-Lösung mit Zinn(II)-chlorid dienen. Dabei entsteht rotes oder violettes kolloidales Gold, das auch als Cassius'scher Goldpurpur bezeichnet wird. Wenn man wenig Blattgold in Königswasser auflöst und zu der entstehenden gelben Gold-Lösung eine Zinnchlorid-Lösung gibt, bildet sich kolloidales Gold:
|
Das
Zinn und seine anorganischen Verbindungen sind zwar weit weniger toxisch
als das Blei, aber nicht ganz unproblematisch.
Sie gelangen vor allem über die Nahrung von zinnhaltigen Lebensmitteln
in den menschlichen Körper. Aber auch zinnhaltige Dentallegierungen
oder Konservendosen können zu einer Exposition führen. Akute
Vergiftungserscheinungen wurden bei Personen beobachtet, die sauren Orangensaft
aus einem Zinngefäß tranken. Anorganische Zinnverbindungen werden
im Magen-Darm-Trakt in geringen Mengen zu organischen Zinnverbindungen
umgewandelt. Diese sind sehr viel toxischer als die anorganischen Zinnverbindungen.
Im Jahre 1954 starben in Frankreich etwa 100 Personen nach der Einnahme
eines Medikaments an einem Gehirnödem. Das Arzneimittel war mit einer
zinnorganischen Verbindung verunreinigt. Dieser Stoff wirkt im Zentralnervensystem
als Gift; er löst Schlafstörungen, Hyperaktivität oder schwere
Krämpfe aus. |
|
Häufigkeit weniger häufig
Elementares Zinn kommt in der Natur sehr selten im gediegenen Zustand oder in natürlichen Legierungen vor, beispielsweise im Yuanjiangit, einer Zinn-Gold-Legierung. Das wichtigste Zinnerz ist der rötlichbraune bis schwarze Kassiterit. Etwas seltener kommt der Stannit vor, der aber als Zinnerz nur eine untergeordnete Bedeutung hat. Die Hauptförderländer der Zinnerze sind China, Peru, Indonesien, Bolivien, Brasilien und Australien.
|
|
Zinn
gehört zu den zehn Metallen des Altertums. Die ältesten Funde
weisen auf die Verwendung von Zinn zusammen mit Kupfer in Bronzelegierungen hin.
Diese traten im 3. Jahrtausend vor Christus in Beilen und Pfeilspitzen
in der Bronzezeit auf. Reines Zinn kannten im 18. Jahrhundert vor Christus
die alten Griechen, aber auch die Chinesen und Japaner im gleichen Zeitraum.
Um 700 vor Christus erzeugten die alten Ägypter Zinnfolien, mit denen
sie Mumien einwickelten. Der römische Geschichtsschreiber Plinius
der Ältere (24–79) beschrieb die Verwendung einer Blei-Zinn-Legierung
zum Verlöten und das Überziehen von Kupfergefäßen
mit einer dünnen Zinnschicht. In den Mittelmeerländern fand sich
kaum Zinnerz, daher musste es aus Britannien oder aus China importiert
werden.
Bis zum 13. Jahrhundert lieferte England den Hauptanteil des europäischen Zinns. Anfang des 12. Jahrhunderts entstanden in Böhmen und in Sachsen die ersten Zinngruben. Zunächst hielt man Zinn für eine Abart von Blei und bezeichnete es als „weißes Blei“, im Gegensatz zum „echten Blei“, dem „schwarzen Blei“. Der Name leitet sich von dem altnordischen Wort tin oder vom althochdeutschen zin ab, was so viel bedeutet wie „Stab“ oder „Platte“. Dem Zinn wurde in der Alchemie das Jupitersymbol zugeordnet. Die beiden Symbole links zeugen davon: 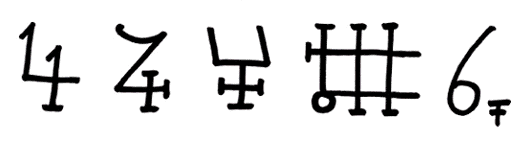
|
|
Das klassische
Lötzinn mit einer Schmelztemperatur von 179 °C enthält 62
Prozent Zinn, 36 Prozent Blei und 2 Prozent Kupfer. Dieses Lötzinn darf nicht mehr gewerblich verwendet werden. Im Hobbybereich ist es aber noch gebräuchlich. Der Zusatz von Bismut senkt die Schmelztemperatur. Im bleifreien Lötzinn ist das Zinn mit bis zu fünf Prozent Silber legiert. Allerdings ist dann die Schmelztemperatur mit etwa 220 °C höher. Der Vorteil
besteht darin, dass keine Bleiabfälle im Elektronikschrot anfallen. Der Dampf beim Löten kann toxische Metalldämpfe enthalten, er besteht aber hauptsächlich aus dem verdampften Flussmittel, das im Lötzinn enthalten ist.
Als Bronze wird eine Legierung bezeichnet, die mindestens 60 % Kupfer und weitere Metalle, aber kein Zink enthält. Die gelblichen Kupfer-Zink-Legierungen bezeichnet man als Messing. Die Bronze für Kanonen enthielt ursprünglich 90 % Kupfer und 10 % Zinn, manchmal auch einen geringen Zinkzusatz. Bei der Glockenbronze beträgt der Zinnanteil um die 20 %. Die abgebildete persische Wasserkanne aus dem 19. Jahrhundert ist nicht aus Bronze. Sie besteht aus Kupfer und ist verzinnt.
Lagermetalle für Achsenlager bei Maschinenwellen enthalten bis zu 90 Prozent legiertes Zinn. Der Zinn-Anteil ermöglicht sehr gute Gleiteigenschaften der Legierung. Ein kleinerer Anteil dient zur Herstellung von Gebrauchsgegenständen aus Zinn wie Becher, Geschirr, Teller
oder Figuren. Die heutigen Verpackungsfolien oder die Lametta für
Christbäume werden nicht mehr aus Zinn, sondern aus Aluminium produziert. Hochreine Zinn-Einkristalle finden wie Silicium in elektronischen Bauteilen Verwendung. Zinnorganische Verbindungen werden in der Landwirtschaft als Fungizide, in der Kunststoffindustrie als Stabilisatoren und in Krankenhäusern als Desinfektionsmittel eingesetzt. Etwa die Hälfte des erzeugten Zinns dient zum Verzinnen von
Eisenblech bei der Herstellung von Konservendosen.
|
|
|