 Teflonverschluss |
 Klare Flüssigkeit Vorkommen Steinkohleteer, Erdöl, Aromastoff in Weintrauben und Kiwis, auch im Baumharz Styrax |
Molmasse 104,150 g/mol AGW 20 ml/m3 (TRGS 900) Dichte 0,9016 g/cm3 Schmelzpunkt −30,65 °C Siedepunkt +145,3 °C Wasserlöslichkeit Konz. bei 25 °C 0,321 g/l Brechungsindex (20°C) 1,5458 Explosionsgrz. 0,9 bis 6,8 Vol.-% (Luft) Flammpunkt +31 °C Zündpunkt +490 °C |
| Piktogramme GHS 02 GHS 07 GHS 08 Gefahr |
Gefahrenklassen
+ Kategorie Entzündbare Flüssigkeiten 3 Ätz-/Reizwirkung auf die Haut 2 Schwere Augenschäd./-reizung 2 Akute Toxizität inhalativ 4 Reproduktionstoxizität 2 Spez. Zielorgan-Toxizität w. Hörorgane 1 |
HP-Sätze (siehe auch Hinweis) H 226, 315, 319, 332, 361D, 372 (Hörorgane) P 210, 260, 280.1-3,7, 302+352, 305+351+338, 308+313, 403+233 Entsorgung G 1 |
| Etikett drucken | Dt. Bezeichnung (Synonyme) |
Engl. Bezeichnung (Synonyme) |
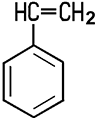
| CAS 100-42-5 | Styrol Styren, Vinylbenzol |
Styrene Vinylbenzene |
Bemerkung
für
Schulen: Styrol reizt Augen, Atemwege, Haut und Schleimhäute. Es
kann auch Störungen im Zentralnervensystem verursachen.
Styrol steht im Verdacht, das Kind im Mutterleib zu schädigen.
Eine krebserzeugende Wirkung ist eventuell möglich, aber noch nicht
eindeutig belegt. Bei wiederholter Exposition können Schäden
am Hör- und Gleichgewichtsorgan auftreten. Das Einatmen der
Dämpfe ist zu vermeiden, daher sollte mit Schutzbrille und
Schutzhandschuhe, sowie im Abzug gearbeitet werden. Wie für alle
Aromaten wird ein besonders dichter Verschluss mit Tefloneinlage
empfohlen. Schülerversuche mit Styrol sind problematisch.
Eigenschaften Styrol ist eine
klare, ölige Flüssigkeit, die süßlich oder
"kunststoffartig" riecht. Sie ist in Wasser nur ganz wenig löslich,
in organischen Lösungsmitteln wie Aceton, Ether oder Ethanol ist
sie sehr gut löslich. Unter Licht- und Wärmeeinwirkung
polymerisiert Styrol zu dem Kunststoff Polystyrol.
Dabei wird die Flüssigkeit zäh und härtet
allmählich aus. Die Zugabe eines Initiators wie Dibenzoylperoxid
beschleunigt den Prozess erheblich. Das im Handel erhältliche
Styrol ist mit Hydrochinon stabilisiert. Styrol ist mit einem Brechungsindex von 1,5458 stark lichtbrechend und übertrifft dabei sogar das Benzol (n=1,5011).
 Dieses Styrol ist leicht polymerisiert, zu erkennen ist die hohe Lichtbrechung. |
| Herstellung Um das Jahr 1830 entdeckte ein
Berliner Apotheker, dass sich das Öl aus dem Styrax-Harz einer
südamerikanischen Baumart in eine zähe Masse verwandelte. Das
Harz wurde namensgebend. Im Jahr 1920 erkannte Hermann Staudinger den makromolekularen Aufbau des Polystyrols. Die industrielle
Produktion begann zehn Jahr später durch die IG Farben in
Ludwigshafen, nachdem man Styrol durch die Dehydrierung von Ethylbenzol
in großen Mengen künstlich produzieren konnte. Das
Ethylbenzol kann relativ einfach mit Hilfe eines
Aluminiumchlorid-Katalysators direkt aus Benzol und Ethylen hergestellt werden. |
| Verwendung Polystyrol war einer der ersten durch Polymerisation hergestellten Kunststoffe. Aufgeschäumtes Polystyrol ist unter dem Namen Styropor bekannt. Styrol dient zur Herstellung weiterer Kunststoffe. Es wird auch als Lösungsmittel eingesetzt. |