und die Eigenschaften von Tensiden
Füllt man ein Sektglas
randvoll mit Wasser, lässt sich noch mehr Wasser in das Glas füllen,
als der eigentliche Volumeninhalt zulassen würde. Die Wasseroberfläche
bildet ein Wölbung nach oben aus, diese ist besonders am Glasrand
sichtbar. Gibt man nun einen Tropfen Geschirrspülmittel auf die Wasseroberfläche
fließt das Wasser über den Glasrand hinab. Dieses Phänomen
kann zuhause selbst in einem kleinen Experiment vorgeführt werden.
Wie kommt das Phänomen im Sektglas zustande und wie lässt sich
die Wirkung eines Tensids erklären?
Das Ablösen von
wasserlöslichem Schmutz wie Salz oder Zucker stellt beim Waschen mit
Wasser kein großes Problem dar. Dieser löst sich im Wasser und
wird dadurch fortgeschwemmt. Problematischer wird es bei wasserunlöslichem
Schmutz wie Fett, Öl, Eiweiß oder Farbflecken von Rotwein oder
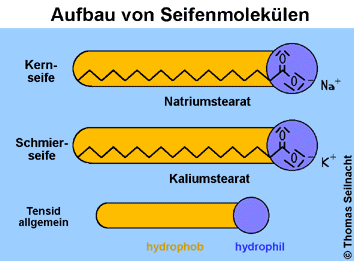
Kaffee. Tenside bringen hydrophile oder wasserliebende
und hydrophobe oder wasserabweisende, also lipophile oder fettliebende Substanzen zusammen. So kann dann auch fetthaltiger Schmutz
durch Wasser abtransportiert werden. Damit dies gelingt, muss ein Tensid-Molekül
aus einem hydrophilen und einem hydrophoben Baustein aufgebaut sein:
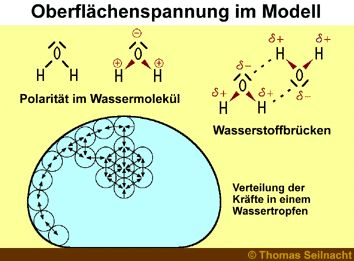
Das Wasser-Molekül
besitzt eine relativ hohe Polarität. Das Sauerstoff-Atom
im Wasser-Molekül zieht aufgrund seiner hohen Elektronegativität
gerne Elektronen an sich heran und benutzt dabei die Elektronen der Elektronenpaarbindungen.
Dadurch ergibt sich eine unterschiedliche Elektronendichte im Wasser-Molekül,
so dass eine Ladungsverschiebung entsteht. Das Wasser-Molekül wird
polar. Die gegensätzlichen Ladungen zwischen
den Wasser-Molekülen ziehen sich gegenseitig an, es entstehen Wasserstoffbrücken. Im Innern der Flüssigkeit ist jedes Wasser-Molekül
von einem anderen Molekül umgeben. Daher heben sich die Kräfte
gegenseitig auf. Anders verhält es sich an der Grenzfläche zwischen
Wasser und einer anderen Phase. An der Oberfläche des Wassers wirken
die Kräfte einseitig. Da die Wasser-Moleküle hier nach oben keine
Nachbarn haben, resultiert daraus eine Kraft, die in das Innere der Flüssigkeit
senkrecht gerichtet ist. Zum Ausgleich bildet daher ein Wassertropfen im
Idealzustand beim freien Fall die Kugelform aus. Die Kugelform bildet die
kleinstmögliche Oberfläche. Liegt der Tropfen auf einem Untergrund
wirken weitere Kräfte - beispielsweise die Schwerkraft - auf den Wassertropfen
ein. So entsteht die typische, eingedellte Tropfenform eines liegenden
Wassertropfens.
Diese Kräfte verursachen
auch die anfangs beschriebene Wölbung im übermäßig
gefüllten Sektglas. Man bezeichnet die Kräfte, die zwischen den
zwei Phasen auftreten, allgemein als Grenzflächenspannung.
An der Wasseroberfläche grenzt die wässrige Phase an eine gasförmige
Phase, im Falle des Wasserglases ist dies die Luft. Die hier auftretende
Oberflächenspannung ist eine spezielle
Form der Grenzflächenspannung zwischen einer flüssigen und einer
gasförmigen Phase. Nur flüssiges Quecksilber hat eine noch höhere
Oberflächenspannung als flüssiges Wasser. Bei unpolaren Flüssigkeiten
wie Hexan oder Diethylether ist die Oberflächenspannung geringer,
bei ihnen verfließen die Tropfen auf einem Untergrund deutlich mehr.
Die Oberflächenspannung
ermöglicht dem Wasserläufer das Laufen auf dem Wasser. Der Wasserläufer
erzeugt eine "Delle" an der Wasseroberfläche, diese wirkt wie von
einer unsichtbaren Haut überzogen. Zum Absinken muss zur Überwindung
der Oberflächenspannung die Oberfläche des Wassers vergrößert
werden, die Schwerkraft vermag dies aufgrund des geringen Gewichts des
Wasserläufers nicht. Manche Gegenstände gehen nicht unter, auch
wenn sie eine höhere Dichte als Wasser haben. Legt man beispielsweise
eine Büroklammer vorsichtig mit Hilfe eines kleinen Filterpapieres
auf die Wasseroberfläche, saugt sich das Filterpapier voll und geht
unter, während die Büroklammer schwimmt:
Die Büroklammer
geht jedoch unter, sobald ein Tropfen eines Tensids zugegeben wird. Das
Tensid verteilt sich sofort in einer dünnen Schicht auf der ganzen
Wasseroberfläche und drückt die Büroklammer vor dem Untergehen
noch kurzzeitig zur Seite. Dieses Phänomen lässt sich demonstrieren,
wenn man Konfetti auf das Wasser streut und dann einen Tropfen Geschirrspülmittel
hinzugibt. Die Papierstückchen werden durch die sich ausbreitende
Tensid-Schicht nach außen gedrückt. Zur
Erklärung auf molekularer Ebene muss man sich vorstellen, dass sich
der hydrophile Anteil der zugegebenen Tensid-Moleküle in Richtung des
Wassers ausrichtet, während der hydrophobe Anteil aus dem Wasser herausragt.
Diese Anordnung ist für die Tensid-Moleküle energetisch besonders
günstig. Gleichzeitig wird aber der Zusammenhalt der Wassermoleküle
gestört, die Oberflächenspannung wird herabgesetzt. Aus diesem
Grund fließt das Wasser auch über den Glasrand des übermäßig
gefüllten Sektglases, sobald man einen Tropfen Geschirrspülmittel
hinzugibt.
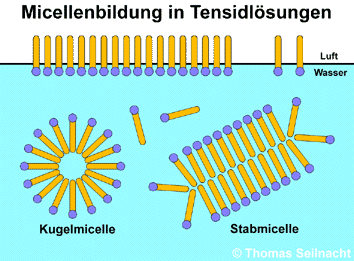
Erst bei der Zugabe von
noch mehr Tensid verteilen sich die Tensid-Moleküle im ganzen Wasser.
Aufgrund ihres molekularen Aufbaus aus hydrophoben und hydrophilen Bauteilen
bilden die im Wasser vorhandenen Tensid-Moleküle eine kugelförmige
Anordnung. Der hydrophile Teil ragt nach außen, während der
hydrophobe Teil nach innen gerichtet ist. So bilden sich Micellen,
die in anionischen Tensiden aus bis zu 100 Tensid-Molekülen aufgebaut
sein können. Bei einer hohen Tensid-Konzentration bilden sich auch
stabförmige Micellen. Im Unterschied zu den echten
Lösungen zeigen Tensid-Lösungen den Tyndall-Effekt.
Dabei wird das Licht an den bis zu 150 Nanometer großen Micellen gebrochen.
Seifenlösungen erscheinen daher im Licht immer ein wenig trübe.
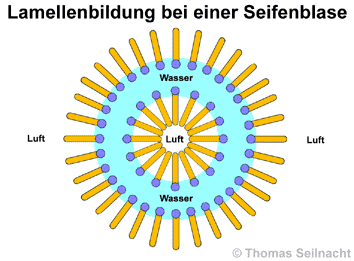
Beim Schütteln einer
Tensid-Lösung dringt Luft ein und Schaumblasen entstehen. Es bildet
sich eine Membran, in der zwei Schichten von Tensid-Molekülen eine
dünne Schicht an Wasser-Molekülen umhüllen. Die Doppelschicht
aus Tensid-Molekülen wird Lamelle genannt.
Seifenblasen entstehen auf diese Art und Weise.
Waschwirkung von Tensiden
Gibt man mit einer Pipette vorsichtig Wasser auf ein Textilgewebe, bilden sich zunächst Wassertropfen. Die Zugabe eines Tensids vermindert die Oberflächenspannung, so dass die Tropfen zerstört und das Wasser in das hydrophobe Gewebe eindringen kann. Bei dieser Benetzung bilden die Wassermoleküle mit den festen Schmutzteilchen und mit dem Gewebe eine Grenzfläche. Diese Benetzung ist die Grundvoraussetzung, damit ein Tensid am Schmutz auf dem Gewebe überhaupt angreifen kann.
Gibt man mit einer Pipette vorsichtig Wasser auf ein Textilgewebe, bilden sich zunächst Wassertropfen. Die Zugabe eines Tensids vermindert die Oberflächenspannung, so dass die Tropfen zerstört und das Wasser in das hydrophobe Gewebe eindringen kann. Bei dieser Benetzung bilden die Wassermoleküle mit den festen Schmutzteilchen und mit dem Gewebe eine Grenzfläche. Diese Benetzung ist die Grundvoraussetzung, damit ein Tensid am Schmutz auf dem Gewebe überhaupt angreifen kann.
Öffnet man ein mit
Öl gefülltes Fläschchen unter Wasser, fließt das Öl
aufgrund der Grenzflächenspannung zwischen den beiden flüssigen
Phasen nicht aus dem Fläschchen heraus, obwohl das Öl die geringere
Dichte als Wasser hat und eigentlich nach oben fließen müsste.
Vermischt man das Wasser mit einem Tensid, wird die Grenzflächenspannung
herabgesetzt und das Öl treibt nach oben.
Gibt man ein angefärbtes
Öl in einem Standzylinder zu Wasser, schwimmt das Öl aufgrund
der geringeren Dichte oben. Nach dem Schütteln trennt sich das Gemisch
nach einiger Zeit wieder. Erst die Zugabe eines Tensids ermöglicht
die Bildung einer Emulsion nach dem
Schütteln:
dem Wasser durch Schütteln vermischen: Es bildet sich eine Emulsion.
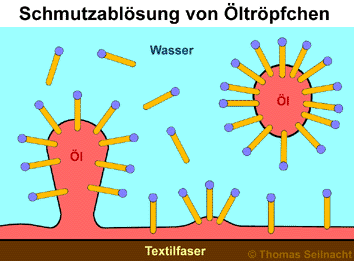
Dabei werden die Öltröpfchen von den Tensid-Molekülen eingehüllt. Der hydrophobe Teil des Tensid-Moleküls ist dem Öltröpfchen zugewandt, während der hydrophile Anteil in Richtung der Wasser-Moleküle zeigt. So werden die Öltröpfchen im fein verteilten Zustand im Wasser gehalten. Beim Reinigen einer ölverschmutzten Faser werden die Ölmoleküle vom Tensid-Molekül ebenfalls „eingehüllt“:
Tenside können auch
feste Schmutzpartikel benetzen. Legt man einen mit Holzkohlepulver verschmutzten
Wollfaden in eine Tensid-Lösung, dann löst sich das Holzkohlepulver
allmählich von der Faser ab, und es bildet sich eine Suspension.
Das Tensid wirkt dabei als Dispergiermittel.
Damit sich der Schmutz vollständig
vom Textilgewebe löst, ist eine mechanische Bewegung notwendig. Außerdem
werden die Vorgänge bei höherer Waschtemperatur erheblich beschleunigt.
Beim Halten der Schmutzteilchen in der Tensid-Lösung spielen auch Ladungs-
und Abstoßungseffekte eine Rolle. Dadurch können sich die abgelösten
Schmutzteilchen nicht mehr zu größeren Bausteinen vereinigen.