 |
 Weißes, kristallines Pulver
|
Molmasse 318,323 g/mol AGW k.A., krebserzeugender Stoff Dichte 1,277 g/cm3 Schmelzpunkt +262,5 °C Wasserlöslichkeit konz. bei 20 °C 0,092 g/l |
| Piktogramme GHS 08 Gefahr |
Gefahrenklassen
+ Kategorie Keimzellenmutagenität 2 Karzinogenität 1B Reproduktionstoxizität FD 2 |
HP-Sätze (siehe auch Hinweis) H 341, 350, 361f P 260, 264, 280.1-3,5,7, 308+313, 405 Entsorgung G 3 |
| Etikett drucken | Dt. Bezeichnung Synonyme (deutsch) |
Engl. Bezeichnung Synonyme (engl.) |
| CAS 77-09-8 | Phenolphthalein 3,3-Bis(4-hydroxyphenyl)-1(3H)- isobenzofuranon |
Phenolphthalein 3,3-Bis(4-hydroxyphenyl)-1(3H)- isobenzofuranone |
Bemerkung
für Schulen: Die momentane GHS-Kennzeichnung, die sich aus den EG-Richtlinien
ergibt, gilt für den Feststoff und für Lösungen ab 1% Konzentration.
Es wird empfohlen, nur mit einer 0,1%igen Lösung zu arbeiten. Die
0,5%ige, käufliche Reagenz kann um den Faktor 5 mit Wasser verdünnt
werden. Wegen des toxischen Potenzials sollte nur verdünnte Phenolphthaleinlösung
als Reagenz für Analysenzwecke in Kleinmengen eingesetzt und gelagert
werden. Für Schülerübungen wird als Ersatzstoff eine Universalindikatorlösung
oder eine Thymolphthaleinlösung empfohlen.
Eigenschaften Reines Phenolphthalein ist ein geruchloses, weißes Pulver, das sich in Wasser nur ganz wenig, in Ethanol und alkalischen Lösungen gut löst. Die klare, ethanolische Lösung eignet sich als Indikatorlösung zum Bestimmen alkalischer Lösungen. Phenolphthalein als Pulver und gebräuchliche Lösung Im sauren und
neutralen
Bereich liegt das Phenolphthalein in der lactoiden Form vor. Bei Zugabe
von Alkalien öffnet sich der Lactonring und man erhält die
chinoide
Form. Bei pH=8,2 erfolgt ein Farbumschlag von Farblos nach Rosa. Durch
Zugabe von Säure wird der Farbumschlag wieder rückgängig
gemacht:
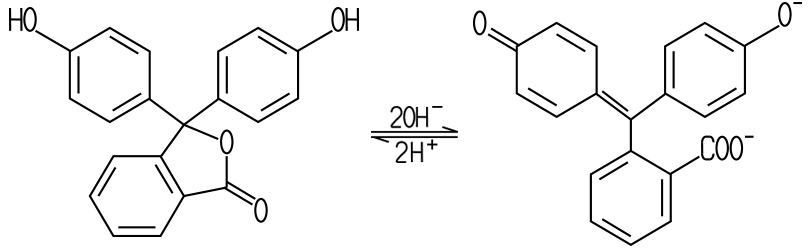 Phenolphthalein: Lactoide Form (links) und chinoide Form (rechts)
Aus diesem Grund eignet
sich Phenolphthalein als Indikator. Bei einem sehr hohen pH-Wert nahe 14 wird es wieder
farblos. Bei einem ganz niedrigen pH-Wert kleiner als Null färbt sich
der Indikator rotorange.
|
| Herstellung Phenolphthalein wird
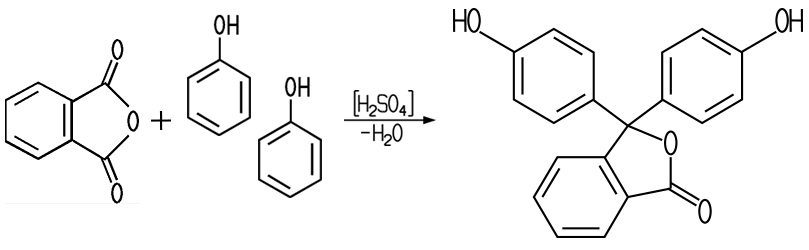
durch das Erhitzen von 1 Mol Phthalsäureanhydrid mit 2 Mol Phenol unter Zugabe von konzentrierter Schwefelsäure dargestellt. Das Phthalsäureanhydrid
kann aus Phthalsäure gewonnen werden. Bei
der sogenannten Friedel-Craft-Reaktion führt die Wasserabspaltung
zum Phenolphthalein:
 |
| Verwendung Phenolphthalein ist ein wichtiger Indikator im Labor. Gebräuchlich sind 0,1%ige oder 1%ige Lösungen in Ethanol oder einem Ethanol-Wasser-Gemisch (>Herstellungsvorschrift). Früher wurde es als Abführmittel verwendet. Heute ist diese Anwendung nicht mehr erlaubt. |