Beim Arbeiten mit Phosphorsäure sind Schutzbrille, Schutzhandschuhe und Schutzkleidung zu tragen. Warme, geschmolzene Phosphorsäure zeigt eine ähnliche Wirkung auf Zellstoff wie konzentrierte Schwefelsäure.
ortho-Phosphorsäure
H3PO4
CAS 7664-38-2
Phosphorsäure
Phosphoric acid
Molmasse
AGW
pKs-Wert (H3PO4)
pKs-Wert (H2PO4−)
pKs-Wert (HPO42−
Dichte
Schmelzpunkt
Siedepunkt
Wasserlöslichkeit
AGW
pKs-Wert (H3PO4)
pKs-Wert (H2PO4−)
pKs-Wert (HPO42−
Dichte
Schmelzpunkt
Siedepunkt
Wasserlöslichkeit
97,995 g/mol
2 mg/m3 (TRGS 900)
+2,16
+7,21
+12,32
1,834 g/cm3
+42,4 °C
+407 °C
100g H2O lösen bei 20 °C 548 g (L)
2 mg/m3 (TRGS 900)
+2,16
+7,21
+12,32
1,834 g/cm3
+42,4 °C
+407 °C
100g H2O lösen bei 20 °C 548 g (L)
Wasserklare, harte Kristalle

Gefahrenklassen + Kategorie
Ätz-/Reizwirkung auf die Haut 1B
Korrosiv gegenüber Metallen 1
(Abstufung bei Verdünnungen)
Ätz-/Reizwirkung auf die Haut 1B
Korrosiv gegenüber Metallen 1
(Abstufung bei Verdünnungen)
HP-Sätze (siehe Hinweis)
H 314, 290
P 260, 280.1–3, 301+330+331, 303+361+353, 305+351+338, 310
Entsorgung Vorbehandlung Säuren/Basen
H 314, 290
P 260, 280.1–3, 301+330+331, 303+361+353, 305+351+338, 310
Entsorgung Vorbehandlung Säuren/Basen
Wasserfreie ortho-Phosphorsäure bildet klare, harte Kristalle, die aus der Luft Wasser anziehen und elektrisch gut leitfähig sind. Erhitzt man die Kristalle über die Schmelztemperatur, schmelzen sie zu einer klaren Flüssigkeit. Diese zerstört zum Beispiel ein Zellstoff-Tuch, wobei eine Verkohlung sichtbar wird. Die Cellulose wird durch eine saure Hydrolyse zu Glucose und weiteren Produkten zersetzt, dann (oder gleichzeitig) erfolgt eine Dehydratisierung, wobei Kohlenstoff und Wasser entsteht. Letzteres wird durch die Phosphorsäure in einem Phosphorsäure-Hydrat aufgenommen. Vereinfacht könnte man auch sagen, dass dem Cellulose-Molekül Wasserstoff und Sauerstoff entzogen werden, so dass Kohlenstoff übrig bleibt.

Lösung und Kristalle (ohne GHS-Kennzeichnung).
Die übliche Phosphorsäure des Handels für den Laborbedarf ist eine 85%-ige Lösung in Wasser. Konzentrierte Phosphorsäure ist keine so starke Säure wie konzentrierte Schwefelsäure. Der pKs-Wert aus dem ersten Schritt der Dissoziation (H3PO4) liegt bei +2,16. Die Phosphorsäure dissoziiert mit Wasser in drei Schritten. Im ersten Schritt entsteht ein Dihydrogenphosphat-Anion H2PO4−, im zweiten Schritt ein Hydrogenphosphat-Anion HPO42− und im dritten Schritt ein Phosphat-Anion PO43−.
Mit Ausnahme ihrer ätzenden Wirkung sind keine gefährlichen Gesundheitsschäden beim Kontakt mit Phosporsäure zu erwarten, der menschliche Körper enthält selbst Phosphorsäure und ihre verwandten Verbindungen. Bei biochemischen Prozessen spielt die Phosphorsäure eine bedeutende Rolle, beispielsweise zum Aufbau der Nucleinsäuren. In der Natur sind die Salze der Phosphorsäure, die Phosphate, weit verbreitet. Knochen enthalten Calciumphosphat, Phosphate sind bedeutende Nährstoffe für die Pflanzen im Boden. Wenn man Phosphorsäure mit Natronlauge neutralisiert, entsteht Natriumdihydrogenphosphat:
Lösung und Kristalle (ohne GHS-Kennzeichnung).
Die übliche Phosphorsäure des Handels für den Laborbedarf ist eine 85%-ige Lösung in Wasser. Konzentrierte Phosphorsäure ist keine so starke Säure wie konzentrierte Schwefelsäure. Der pKs-Wert aus dem ersten Schritt der Dissoziation (H3PO4) liegt bei +2,16. Die Phosphorsäure dissoziiert mit Wasser in drei Schritten. Im ersten Schritt entsteht ein Dihydrogenphosphat-Anion H2PO4−, im zweiten Schritt ein Hydrogenphosphat-Anion HPO42− und im dritten Schritt ein Phosphat-Anion PO43−.
Erster Schritt: H3PO4 + H2O 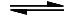 H2PO4− + H3O+
H2PO4− + H3O+
Zweiter Schritt: H2PO4− + H2O 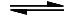 HPO42− + H3O+
HPO42− + H3O+
Dritter Schritt: HPO42− + H2O 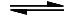 PO43− + H3O+
PO43− + H3O+
Mit Ausnahme ihrer ätzenden Wirkung sind keine gefährlichen Gesundheitsschäden beim Kontakt mit Phosporsäure zu erwarten, der menschliche Körper enthält selbst Phosphorsäure und ihre verwandten Verbindungen. Bei biochemischen Prozessen spielt die Phosphorsäure eine bedeutende Rolle, beispielsweise zum Aufbau der Nucleinsäuren. In der Natur sind die Salze der Phosphorsäure, die Phosphate, weit verbreitet. Knochen enthalten Calciumphosphat, Phosphate sind bedeutende Nährstoffe für die Pflanzen im Boden. Wenn man Phosphorsäure mit Natronlauge neutralisiert, entsteht Natriumdihydrogenphosphat:
H3PO4 + NaOH  NaH2PO4 + H2O
NaH2PO4 + H2O
Verbrennt man weißen oder roten Phosphor in einer großen Glasglocke, die in einem Wasserbehälter steht, dann bildet sich ein weißer Nebel. Das so gebildete Phosphor(V)-oxid P4O10 löst sich im Wasser unter Bildung von Phosphorsäure:
Ist das Wasser mit Universalindikatorlösung versetzt, erkennt man die Bildung einer Säure an der Rotfärbung. Gleichzeitig steigt der Wasserspiegel innerhalb der Glocke an, da bei der Verbrennung von Phosphor Luftsauerstoff verbraucht wird.

Beim Verbrennen des Phosphors bildet sich ein weißer Nebel.
Das Produkt Phosphor(V)-oxid löst sich im Wasser mit saurer Reaktion.
Film
Die industrielle Gewinnung erfolgt aus dem Mineral Apatit. Durch eine Flotation wird das erzhaltige Gestein zunächst konzentriert und danach mit Schwefelsäure umgesetzt:
I.) P4 + 5 O2  P4O10
P4O10
II.) P4O10 + 6 H2O 4 H3PO4
4 H3PO4
II.) P4O10 + 6 H2O
Ist das Wasser mit Universalindikatorlösung versetzt, erkennt man die Bildung einer Säure an der Rotfärbung. Gleichzeitig steigt der Wasserspiegel innerhalb der Glocke an, da bei der Verbrennung von Phosphor Luftsauerstoff verbraucht wird.

Beim Verbrennen des Phosphors bildet sich ein weißer Nebel.
Das Produkt Phosphor(V)-oxid löst sich im Wasser mit saurer Reaktion.
Film
Die industrielle Gewinnung erfolgt aus dem Mineral Apatit. Durch eine Flotation wird das erzhaltige Gestein zunächst konzentriert und danach mit Schwefelsäure umgesetzt:
Ca3(PO4)2 + 3 H2SO4  3 CaSO4 + 2 H3PO4
3 CaSO4 + 2 H3PO4
Die Phosphorsäure dient in großem Umfang zur Herstellung von Düngemitteln. Früher verwendete man die Salze der Phosphorsäure, die Phosphate, als Enthärter in Waschmitteln. Phosphorsäure wird auch als Reinigungsmittel in Rostumwandlern oder in flüssigen WC-Reinigern verwendet, sowie zum Säuern von Softdrinks, beispielsweise in Coca Cola. In der Elektronik benötigt man sie zum Ätzen von Platinen.
Weitere Infos und Medien
Der Säurebegriff im Haushalt und in der Chemie, Phosphate
Weitere Infos und Medien
Der Säurebegriff im Haushalt und in der Chemie, Phosphate
© Thomas Seilnacht / Benutzerhandbuch / Lizenzbestimmungen / Impressum / Datenschutz / Literaturquellen